具有优良的稳定性和较低的耐药敏感性的纳米酶在抗菌领域中表现出了重要的应用潜力。然而,由于催化生成的活性氧(ROS)的靶向能力较低且催化活性不足,因此其难以有效应对复杂伤口环境中的多重耐药生物(MDROs)。有鉴于此,安徽医科大学王咸文教授和陈旭林教授通过一种简单的方法成功构建了化学稳定的铜-没食子酸-万古霉素(CuGA-VAN)纳米针,并将其用于靶向细菌。
本文要点:
(1)这些纳米针具有类OXD和类GSH-px的双酶活性,可产生ROS并诱导细菌发生铜死亡样死亡,以消除MDRO感染。体外实验结果表明,在耐甲氧西林金黄色葡萄球菌(MRSA)的细胞壁骨架中,GA的游离羧酸能够与磷壁酸的游离氨发生反应。因此,CuGA-VAN纳米针可以在液体环境中快速“捕获”MRSA,并在细菌表面释放ROS、VAN和Cu2+,打破MRSA屏障,破坏生物膜。
(2)此外,CuGA−VAN也能够有效促进创面修复细胞的增殖和血管生成,在保证生物安全性的同时促进创面愈合。转录组测序结果显示,高度内化的Cu2+会产生铜过载毒性,下调与细菌乙醛酸循环、三羧酸循环和氧化呼吸链相关的基因,并诱导细胞质中的脂质过氧化,导致细菌性铜死亡样死亡。综上所述,该研究构建的CuGA−VAN能够触发实现靶向、药物释放、基于ROS催化的抗菌活性和铜死亡样死亡的级联反应。有望为治疗耐多药细菌感染提供一种新的思路。
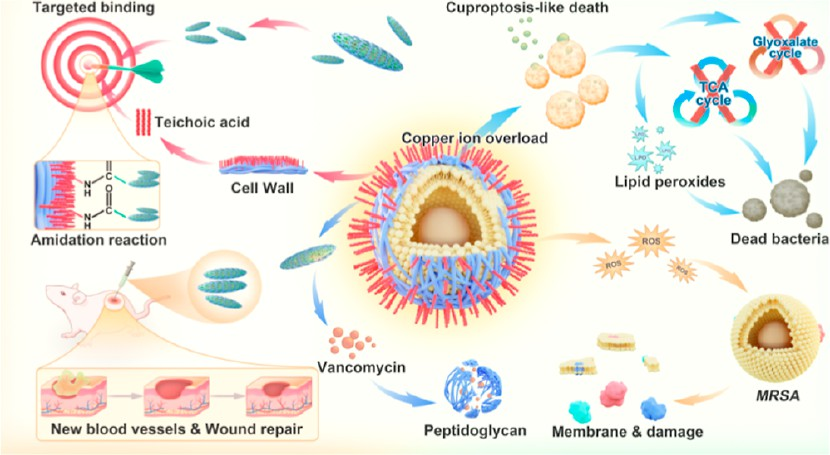
Zhiyuan Hu. et al. Nanoarchitectonics of in Situ AntibioticReleasing Acicular Nanozymes for Targeting and Inducing Cuproptosis-like Death to Eliminate Drug-Resistant Bacteria. ACS Nano. 2024
DOI: 10.1021/acsnano.4c06565
https://pubs.acs.org/doi/10.1021/acsnano.4c06565



















