放疗(RT)的疗效会受到X射线吸收不充分、活性氧产生效率低下、免疫抑制因子上调和还原性肿瘤微环境(TME)等因素的影响。有鉴于此,芝加哥大学林文斌教授开发了一种靶向线粒体。负载洋地黄皂苷(Dig)的纳米级金属有机框架(Th-Ir-DBB/Dig),其能够在低剂量X射线照射下产生强大的抗肿瘤作用。
本文要点:
(1)Th-Ir-DBB由Th6O4(OH)4二级构建单元(SBUs)和光敏性Ir(DBB)(ppy)22+(Ir-DBB,DBB=4,4′-二(4-苯甲酸)−2,2′-联吡啶)构建而成,其可通过高原子序数SBUs的强效放射增敏性能产生羟基自由基以及对Ir-DBB配体的有效激发产生单线态氧,进而能够表现出显著的RT-放射动力学治疗(RDT)效果。
(2)Th-Ir-DBB/Dig可在酸性TMEs中释放洋地黄皂苷,并通过消耗葡萄糖和谷胱甘肽触发癌细胞双硫死亡,使癌细胞对RT-RDT更加敏感。释放的洋地黄皂苷可同时通过消耗胆固醇下调癌细胞和T细胞中的多个免疫检查点。实验结果表明,在X射线照射下,Th-Ir-DBB/dig可诱导产生较强的抗肿瘤免疫,以有效抑制结肠癌和乳腺癌小鼠模型的肿瘤生长。
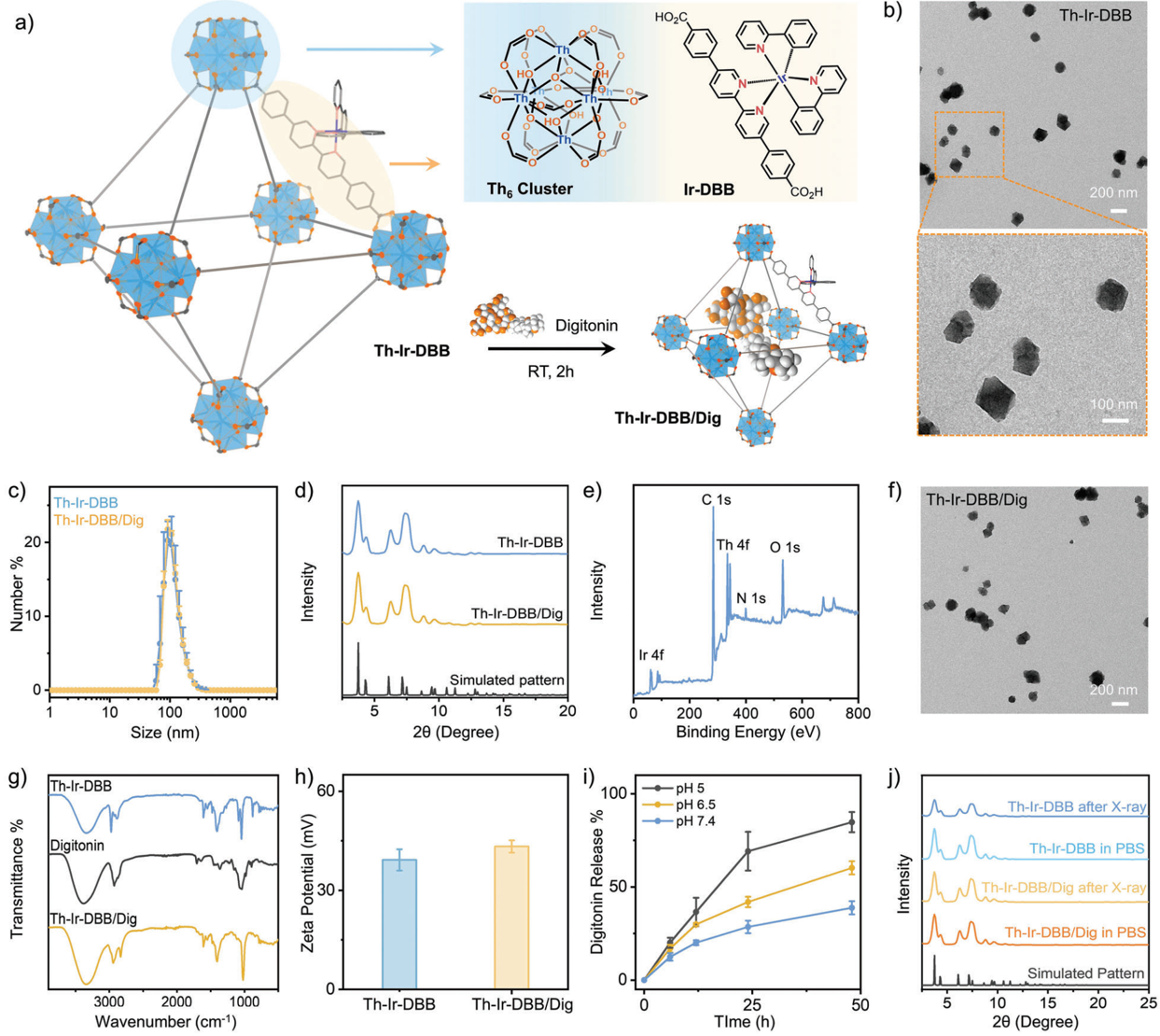
Wenyao Zhen. et al. Digitonin-Loaded Nanoscale Metal–Organic Framework for Mitochondria-Targeted Radiotherapy-Radiodynamic Therapy and Disulfidptosis. Advanced Materials. 2024
DOI: 10.1002/adma.202405494
https://onlinelibrary.wiley.com/doi/10.1002/adma.202405494



















