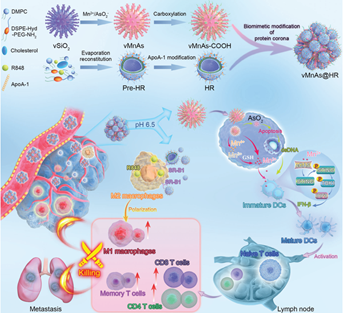
砷制剂在对抗白血病方面具有巨大的应用潜力,但其治疗实体肿瘤的效率仍有待提高,主要原因在于其清除速度快,靶向能力低。形态调控可以增强纳米颗粒与细胞膜之间的相互作用。有鉴于此,山东第一医科大学王昌龙教授、邵凤英教授和李照伟教授开发了一种可拆卸蛋白冠修饰的类病毒锰-砷纳米药物(vMnAs@HR),并将其用于实现安全靶向给药和协同砷治疗。
本文要点:
(1)实验构建了类病毒锰-砷纳米颗粒(vMnAs),然后利用负载R848的HDL(HR)蛋白冠对其进行修饰。静脉注射后,HR蛋白冠能够利用HDL与其受体SR-BI之间的相互作用稳定、主动地靶向肿瘤组织。研究发现,在肿瘤中积累后,HR会被“拆卸丢弃”并与巨噬细胞发生相互作用以实现促炎表型调节,而再暴露的vMnAs则可以利用合理设计的尖刺形态有效地增强内吞作用。
(2)实验结果表明,在肿瘤细胞凋亡过程中释放的双链DNA(dsDNA)和锰离子可以协同激活DCs的环鸟苷单磷酸腺苷单磷酸合成酶(cGAS)-干扰素基因刺激因子(STING)信号通路,从而实现系统性免疫激活。综上所述。该研究构建的形态可转化纳米药物能够实现安全有效的砷递送和协同性砷治疗。
Haina Tian. et al. Dismountable Protein Corona-Modified Virus-Like Manganese-Arsenic Nanomedicine Enables Safe and Targeted Delivery for Synergistic Arsenotherapy. Advanced Materials. 2024
DOI: 10.1002/adma.202408361
https://onlinelibrary.wiley.com/doi/10.1002/adma.202408361



















