纳米技术在临床实践应用中具有巨大的应用价值。然而,目前纳米药物的研究主要致力于开发能够作为递送载体的纳米颗粒,以最大限度地提高药物的生物利用度,而很少关注其直接调节生理过程的潜力。受未降解物质过度积累引起的溶酶体肿胀的启发,安徽医科大学刘琦教授、潘佩教授和南开大学刘阳教授设计了一种靶向溶酶体的聚集纳米颗粒(LTANP),并将其用于癌症治疗。
本文要点:
(1)LTANP可通过合理设计的表面组成、性质和颗粒间相互作用实现高效的肿瘤积累以及在癌细胞溶酶体中的选择性靶向聚集,导致溶酶体发生不可缓解的肿胀,最终诱导癌细胞溶酶体膜透化(LMP)。研究发现,纳米颗粒聚集介导的LMP可以通过损害自噬-溶酶体途径有效触发免疫原性细胞死亡(ICD),进而能够在黑色素瘤模型中引发强大的抗肿瘤免疫反应,使肿瘤免疫原性由“冷”转“热”。
(2)实验结果表明,LTANP可与临床批准的程序性死亡配体-1(PD-L1)抗体相联合以进一步激活T细胞介导的抗肿瘤免疫,显著提高抗肿瘤性能,抑制肿瘤的复发和转移。综上所述,该研究设计了一种能够直接对抗癌症的新型纳米结构,并为发展基于纳米粒子的先进癌症疗法提供了新的见解。
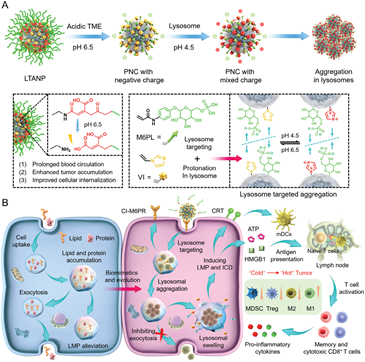
Yumeng Xing. et al. Lysosome Targeted Nanoparticle Aggregation Reverses Immunosuppressive Tumor Microenvironment for Cancer Immunotherapy. Advanced Materials. 2024
DOI: 10.1002/adma.202412730
https://onlinelibrary.wiley.com/doi/10.1002/adma.202412730



















