mRNA疫苗在预防和治疗传染病等方面的成功应用彰显了它们作为治疗性癌症疫苗的重要潜力。然而,与感染性疾病不同的是,抗肿瘤治疗(特别是对实体瘤而言)需要激活更强大的细胞和体液免疫才能产生良好的临床疗效。有鉴于此,中国科学院动物研究所魏妥研究员和北京大学程强研究员开发了一种脾脏靶向mRNA疫苗(Mn@mRNA-LNP),其能够将编码肿瘤抗原的mRNA和锰佐剂(Mn2+)同时递送到脾脏的树突状细胞(DCs)。
本文要点:
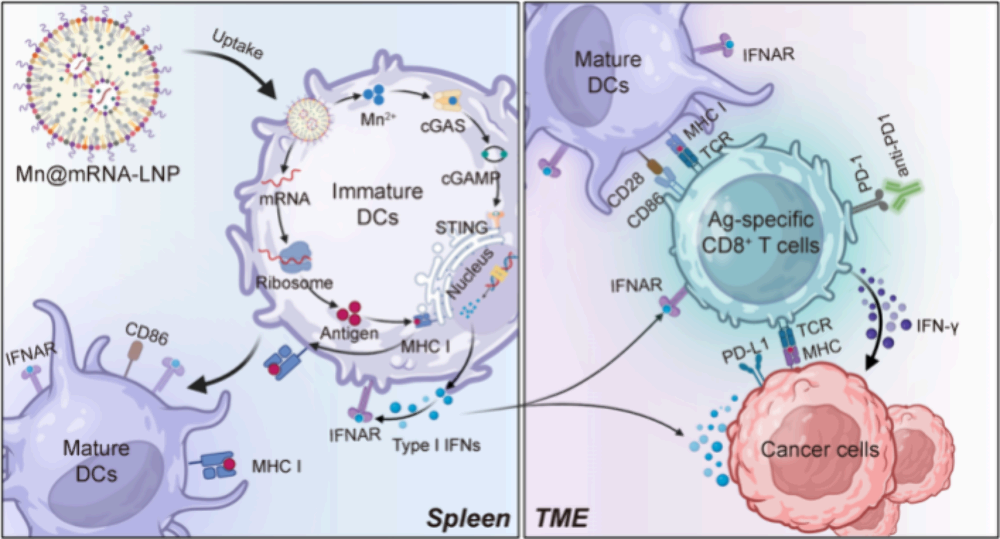
(1)该递送系统可促进DC成熟和表面抗原呈递,并刺激细胞毒性T细胞的产生。在系统中共递送的Mn2+能够作为安全有效的免疫佐剂,激活干扰素基因刺激因子(STING)信号通路,促进I型干扰素的分泌,以进一步增强抗原特异性T细胞应答。在已建立的黑色素瘤和结肠肿瘤模型以及肿瘤切除术后复发模型中,Mn@mRNA-LNP能够有效抑制肿瘤进展。
(2)实验结果表明,Mn@mRNA-LNP联合免疫检查点抑制剂能够实现对小鼠肿瘤的完全抑制,并显著延长小鼠的总体生存期。综上所述,该研究设计的“All-in-One”mRNA疫苗可通过改善脾脏靶向和免疫激活显著增强抗肿瘤免疫应答,有望为治疗性mRNA疫苗的临床转化提供一个新的策略。
Zijin Luo. et al. Spleen-Targeted mRNA Vaccine Doped with Manganese Adjuvant for Robust Anticancer Immunity In Vivo. ACS Nano. 2024
DOI: 10.1021/acsnano.4c09902
https://pubs.acs.org/doi/10.1021/acsnano.4c09902



















