利用光生成活性氧(ROS)刺激一氧化碳(CO)的可控释放是一种极具发展前景的癌症治疗方法。然而,传统光敏剂在乏氧肿瘤微环境中的CO释放率低和ROS生成不足等问题仍会导致该策略的应用严重受限。有鉴于此,华南理工大学冯光雪教授和南开大学丁丹教授通过共包封有机AIE光敏剂(PS)和CO前药(Fe3(CO)12)开发了一种高效的纳米平台(TPyNO2−FeCO NPs),其能够实现光触发的ROS生成和CO释放,以用于协同光动力治疗(PDT)和CO气体治疗。
本文要点:
(1)实验通过引入α-光诱导电子转移(α-PET)过程使得TPyNO2能够高效地产生I型和II型ROS。当以4-硝基苄基单元作为典型的PET供体时,分子内α-PET过程不仅可以抑制辐射衰变,使激发态能量重新定向到系间窜越以形成更多的三重态,而且能够促进电子的分离和转移过程,以产生自由基型ROS。研究发现,聚集态TPyNO2具有优越的单线态氧、超氧阴离子和羟基自由基生成性能。
(2)在光照射下,TPyNO2−FeCO NPs可通过I型和II型双模态ROS介导的过程实现CO的可控靶向释放,以克服传统CO释放系统的局限性。此外,由于释放的CO能够通过诱导细胞内氧化应激、使线粒体膜电位去极化和抑制ATP的产生等机制导致细胞内ROS的进一步生成,因此TPyNO2−FeCO NPs可以实现自加速的ROS-CO-ROS回路。体内外实验结果表明,协同的PDT和CO气体治疗具有良好的抗肿瘤性能。综上所述,该研究工作为开发先进的PS提供了重要的见解,所构建的TPyNO2−FeCO NPs纳米平台在实现安全有效的抗肿瘤应用方面具有广阔的前景。
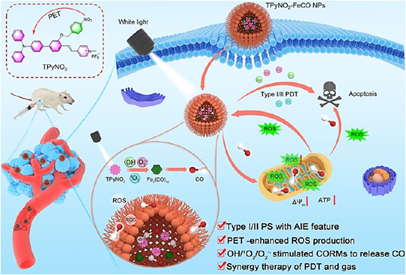
Yuewen Yu. et al. Dual-Mode Reactive Oxygen Species-Stimulated Carbon Monoxide Release for Synergistic Photodynamic and Gas Tumor Therapy. ACS Nano. 2024
DOI: /10.1021/acsnano.4c10277
https://pubs.acs.org/doi/10.1021/acsnano.4c10277



















