炎症免疫微环境是动脉粥样硬化斑块发生侵蚀和破裂的重要原因。近红外二区(NIR-II)荧光成像具有连续监测斑块免疫微环境时空变化的重要潜力。有鉴于此,温州医科大学纪建松教授、Lingchun Lv新加坡国立大学陈小元院士和Jianhua Zou构建了三种不同的基于BBT-2FT的NIR-II探针:VHPK/BBT-2FT NPs(VHPK是靶向血管细胞粘附分子-1的特异性肽);iNOS/BBT-2FT NPs(可通过诱导型NO合酶(iNOS)抗体调节M1巨噬细胞极化)和Arg-1/BBT-2FT(用于平衡M1巨噬细胞的炎症反应)。
本文要点:
(1)这些示踪剂能够通过NIR-II成像精准示踪动脉粥样硬化斑块以及M1和M2巨噬细胞。VHPK/BBT-2FT NPs能够在各个阶段准确地示踪动脉粥样硬化斑块。Arg-1/BBT-2FT NPs可在过氧化物酶体增殖物激活受体γ(PPAR-γ)、信号传导子及转录激活子(STAT)6以及ATP结合盒转运体A1(ABCA1)发生上调的早期斑块微环境中精确定位M2巨噬细胞,表明M2巨噬细胞极化对于早期斑块脂质清除而言至关重要。iNOS/BBT-2FT NPs则能够准确地示踪晚期斑块微环境中的M1巨噬细胞。
(2)实验结果表明,在晚期乏氧斑块微环境中,M1巨噬细胞极化可通过厌氧糖酵解代谢和焦亡诱导炎症微环境的形成。免疫学研究和NIR-II成像结果显示,乏氧诱导的巨噬细胞代谢重编程是动脉粥样硬化斑块免疫微环境发生动态变化的关键因素。综上所述,该研究开发了一种能够对动脉粥样硬化中的不稳定斑块破裂进行实时诊断和临床预防的新策略。
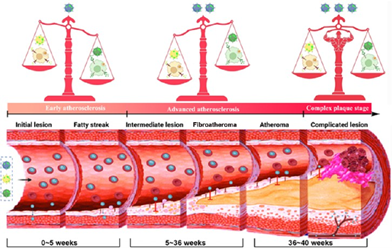
Lin Shen. et al. NIR-II Imaging for Tracking the Spatiotemporal Immune Microenvironment in Atherosclerotic Plaques. ACS Nano. 2024
DOI: 10.1021/acsnano.4c10739
https://pubs.acs.org/doi/10.1021/acsnano.4c10739



















