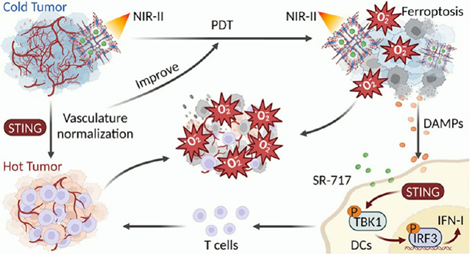
光动力疗法(PDT)具有提高治疗精度和治疗安全性的重要潜力。开发由近红外二区(NIR-II)激光活化的光敏剂能够增强深层组织穿透、减少组织吸收和光毒性。然而,PDT的疗效仍会受到乏氧肿瘤微环境(主要是由不规则的肿瘤血管系统引起)的阻碍。干扰素基因刺激因子(STING)通路具有免疫激活作用,并且与血管正常化有关。有鉴于此,南洋理工大学赵彦利教授和太原市中心医院牛旭平教授将STING激动剂(SR-717)负载到铁-四羟基-1,4-苯醌(Fe-THBQ)金属有机框架中,开发了一种纳米平台(Fe-THBQ/SR)。
本文要点:
(1)Fe-THBQ是一种有效的NIR-II光敏剂,其在1064 nm激光照射下能够产生大量活性氧(ROS)。ROS可下调热休克蛋白的表达,以促进温和光热治疗(mild-PTT),并且能够通过消耗谷胱甘肽(GSH)/谷胱甘肽过氧化物酶4促进铁死亡。
(2)实验结果表明,Fe-THBQ/SR可在GSH刺激下释放SR-717,其能够协同ROS介导的双链DNA泄漏增强STING激活。该过程有助于实现肿瘤血管的正常化和乏氧缓解,以提高PDT的疗效。综上所述,该研究构建了一种单激光触发的多功能纳米平台,其能够实现NIR-II PDT和NIR-II mild-PTT,并且可以同时结合STING激活,以形成强化循环,协同增强肿瘤细胞的免疫原性,重塑免疫抑制的肿瘤微环境,增加T淋巴细胞浸润,改善肿瘤治疗结果。
Huan Zhao. et al. A Second Near-Infrared Window-Responsive Metal−Organic-Framework-Based Photosensitizer for Tumor Immunotherapy via Synergistic Ferroptosis and STING Activation. Journal of the American Chemical Society. 2025
DOI: 10.1021/jacs.4c13241
https://pubs.acs.org/doi/10.1021/jacs.4c13241



















