溶酶体靶向嵌合体(LYTACs)是一种通过劫持溶酶体靶向受体来降解细胞外和膜相关致病性蛋白的治疗策略。然而,LYTAC的抗肿瘤作用仍会受到肿瘤积累不足和非特异性激活等问题的限制。此外,实现LYTACs和其它治疗方式的协同作用对于增强疗效至关重要。有鉴于此,安徽医科大学Qi Liu和南开大学刘阳研究员开发了一种双功能LYTAC纳米平台(NLTC),并将其用于实现肿瘤选择性蛋白降解和增强癌症免疫治疗。
本文要点:
(1)研究者通过合理控制表面组成使得NLTC可以有效地将细胞外蛋白或膜蛋白通过不依赖阳离子的甘露糖6-磷酸受体转运到溶酶体中进行降解。经过表面修饰后,实验构建了能够在肿瘤组织中有效积累的NLTC,其可以避免靶外肿瘤毒性。此外,NLTC的合成方法也普遍适用于多种酶。
(2)因此,研究者将过氧化氢酶(CAT)封装在NLTC中,以协同降解癌细胞表面的程序性死亡配体-1(PD-L1)。实验结果表明,该策略能够缓解免疫抑制性肿瘤微环境,实现有效的癌症免疫治疗,显著抑制B16F10荷瘤小鼠的肿瘤生长、复发和转移。综上所述,该研究工作构建了一种双功能LYTAC纳米平台,其不仅可以进行组织选择性蛋白质降解,还可以与其它治疗方式相集成,有望为推动LYTAC技术的临床应用提供新的见解。
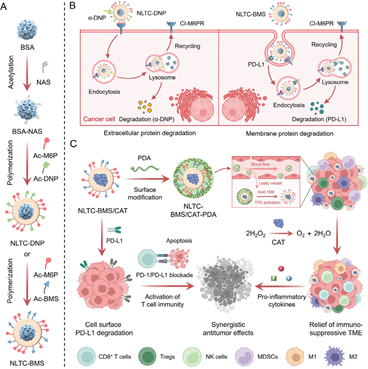
Yumeng Xing. et al. A Bifunctional Lysosome-Targeting Chimera Nanoplatform for Tumor-Selective Protein Degradation and Enhanced Cancer Immunotherapy. Advanced Materials. 2025
DOI: 10.1002/adma.202417942
https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202417942



















